- نمونه سوال4فصل اول شیمی دوازدهم
- نمونه سوال3فصل اول شیمی دوازدهم
- کلوپ بازی بروز(اندیشه)
- کلوپ بازی بروز
- آموزش خصوصی شیمی دوره دبیرستان
- نمونه سوال امتحان نهایی شیمی دوازدهم
- بارم بندی وبودجه بندی شیمی دوازدهم
- امتحان نهایی پایه دوازدهم
- نمونه سوال2فصل اول شیمی دوازدهم
- نمونه سوال1فصل اول شیمی دوازدهم
خانه ی شیمیChemistry home
آموزش شیمی دوره دبیرستان ، پیش دانشگاهی وکنکور
درجدول دوره ای عناصرگوگردشش الکترون واکسیژن هم شش الکترون درلایه ظرفیت داردجمع الکترونهای ظرفیت دریون سولفات بادوبارمنفی برابر32 الکترون می شود.
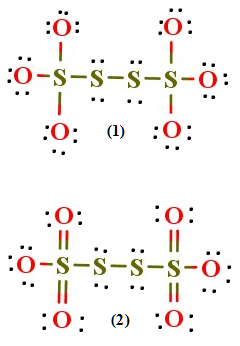
اتم گوگردرادروسط قرارداده چهاراتم اکسیژن رادراطراف آن قرارمی دهیم وبین اتم گوگردباهریک ازاتم های اکسیژن دوالکترون قرارمی دهیم بنابراین هشت الکترون ظرفیت به کاررفته واز32 الکترون ظرفیت 24 الکترون باقی می ماند
دراطراف هراتم اکسیژن شش الکترون(ناپیوندی) قرارمی دهیم تاهریک ازاتم هابه آرایش هشت تایی برسنددراین ساختار(A)همه ی اتم هابه آرایش هشت تایی رسیده اند.
اتم گوگرددردوره ی سوم جدول دوره ای قرارداردبنابراین بایدبارهای قراردادی رابررسی کنیم.
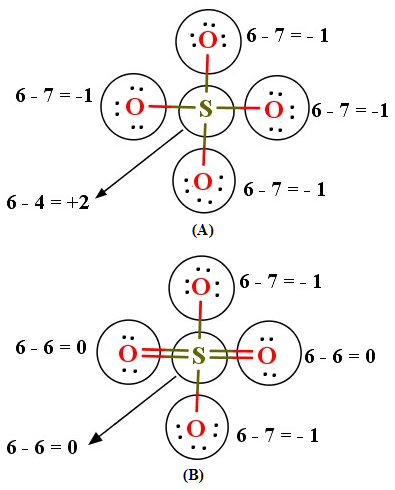
بارقراردادی روی اتم گوگردراحساب می کنیم اتم گوگرددرگروه16 جدول دوره ای است بنابراین 6 الکترون درلایه ظرفیت داردکه همه آنهادرپیوندهای کووالانسی به اشتراک گذاشته شده اندالکترون های پیوندی اتم گوگرد8الکترون می باشدکه تقسیم بر2کنیم 4الکترون سهم اتم گوگردو6منهای4برابر2+خواهدشدبنابراین بارقراردادی اتم گوگردبرابر2+می باشد
اتم اکسیژن هم درگروه 16قراردادرکه 6الکترون درلایه ظرفیت دارددراین ساختارهراتم اکسیژن شش الکترون ناپیوندی و2الکترون پیوندی داردکه تقسیم بر2کنیم سهم هراتم اکسیژن یک الکترون می باشدپس درمجموع سهم هراتم اکسیژن7الکترون (پیوندی وناپیوندی) می باشدبرای محاسبه ی بارقراردادی اتم اکسیژن6رامنهای 7می کنیم بارقراردادی برابر1- می شود
مجموع بارهای قراردادی 4اتم اکسیژن ویک اتم گوگردبرابر2-می شود.
حالابایدکاری کنیم بارقراردادی اتم هاتاحدامکان صفرشودبنابراین ساختارلوویس دیگری رارسم می کنیم که درآن بارقراردادی اتم های بیشتری صفرباشدباتوچه به این که دراین ساختاردوبارمثبت روی اتم گوگردقرارداردبنابراین می توانیم الکترون هایی راازلایه ظرفیت اکسیژن به صورت ناپیوندی هستندکم کنیم وبه الکترون های پیوندی اضافه کنیم وپیونددوگانه تشکیل شوداگراین کاررادوبارانجام دهیم دوپیونددوگانه تشکیل می شودوماازدوبارمثبت روی اتم گوگردخلاص می شویم. حالادراین ساختارجدید(B)یک باردیگربارهای قراردادی راحساب می کنیم بارقراردادی روی اتم گوگردبرابرصفروبارقراردادی اتم های اکسیژن که بااتم گوگرد پیونددوگانه دارندبرابرصفروبارقراردادی هریک ازاتم های دیگراکسیژن برابرمنهای یک می شودوجمع بارهای قراردادی دراین ساختاربرابر2-خواهدبودکه باباریون مطابقت دارد.این یک ساختارلوویس بهتری است چون بیشتربارهای قراردادی اتم هادرآن برابرصفرمی باشند.
برای بررسی درستی یک ساختارلوویس ویاانتخاب بهترین ساختارلوویس ازبین دویاچندساختارممکن برای یک ترکیب بارقراردادی آن راحساب می کنیم .
- ساختاری که بارقراردادی آن (هریک ازاتم ها)به صفرنزدیک ترباشدبهترین ساختاراست .
-برای یونهای مثبت یامنفی مچموع بارهای قراردادی بایدبرابرباریون باشد.
-وقتی باترکیب های عناصردوره ی سوم به بعدسروکارداریم بارقراردادی رابررسی می کنیم.
محاسبه ی بارقراردادی:
بارقراردادی رامی توان بایکی ازروش های زیرحساب کرد.
1- (تعدادالکترون هادراطراف اتم درمولکول)-(تعدادالکترون های لایه ظرفیت دراتم خنثی)=بارقراردادی
2- (تعدادالکترون های ناپیوندی)-(نصف تعدادالکترون های اتم درپیوندهای کووالانسی)- ( تعدادالکترون های لایه ظرفیت دراتم خنثی)=بارقراردادی
3- (تعدادالکترون های ناپیوندی)-( تعدادپیوندهای کووالانسی)- ( تعدادالکترون های لایه ظرفیت دراتم خنثی)=بارقراردادی
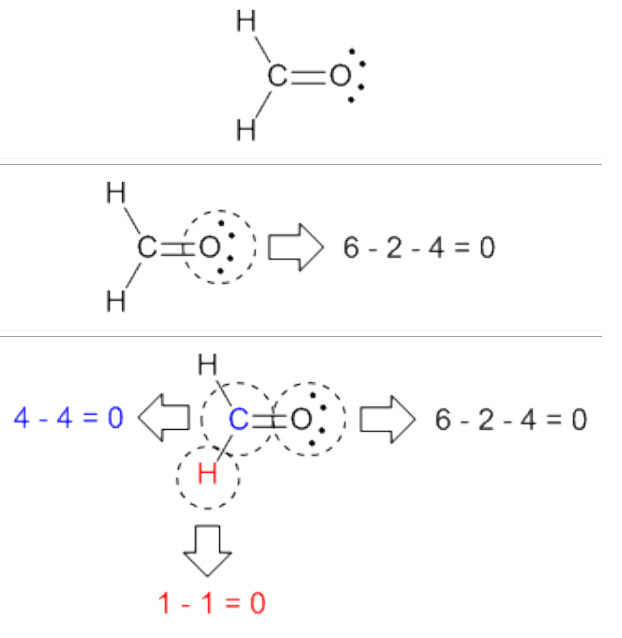
4- (a) اطراف اتم موردنظریک دایره رسم می کنیم.
(b) تعدادالکترون های این اتم رادرون دایره شمارش می کنیم(الکترون های پیوندی مشترک هستند).
(c) الکترون های درون دایره – تعدادالکترون های لایه ظرفیت اتم =بارقراردادی اتم
مراحل کلی نوشتن ساختارهای لوویس:
1-رسم آرایش اتم هانسبت به یکدیگر:
1-1)برای ترکیب هایی بافرمول عمومی ABn اتمی که شماره گروه پایین تری دارددرمرکزقرارمی گیرد.
(معمولا این اتم الکترونگاتیوی کمتری دارد)
2-1)اگراتم هاشماره گروه یکسانی دارنداتمی که شماره دوره بزرگتری دارددرمرکزقرارمی گیرد.
3-1)اتم H یک پیوندتشکیل می دهدبنابراین به عنوان اتم مرکزی قرارنمی گیرد.
2-تعدادالکترونهای ظرفیت همه اتمهاراجمع می کنیم.
1-2)برای آنیونهابه ازای هربارمنفی یک الکترون به مجموع الکترون های ظرفیت اضافه می کنیم.
2-2)برای کاتیون هابه ازای هربارمثبت یک الکترون ازمجموع الکترون های ظرفیت کم می کنیم.
3-ازهراتم اطراف یک پیوندیگانه به سمت اتم مرکزی رسم می کنیم.
4-به ازای هرپیوندیگانه دوالکترون ازمجموع الکترون های ظرفیت کم می کنیم.
5-الکترون های ظرفیت باقی مانده رابه صورت جفت بین اتم هاتقسیم می کنیم تاهراتم 8 الکترون داشته باشد(اتم H دوالکترون می گیرد).
1-5)جفت الکترون های ناپیوندی راابتداروی اتم های اطراف قرارمی دهیم.
2-5)الکترون های باقی مانده راروی اتم مرکزی قرارمی دهیم.
6-اگراتم مرکزی 8 الکترون نداشت جفت الکترون های ناپیوندی رو ی اتم های اطراف رابه جفت الکترون های پیوندی بااتم مرکزی تبدیل می کنیم تاپیوندهای چندگانه تشکیل شود.
7-بررسی می کنیم که هراتم 8 الکترون ظرفیت(اتم H 2 الکترون)داشته باشد.
دانش آموزانی که به دنبال رسم صحیح ساختارلوویس می باشنددرقسمت پیوندهای روزانه می توانندبه نرم افزاری دسترسی پیداکنندکه این ساختارهارارسم می کند،پس ازواردشدن درسایت مربوطه مقابل کلمه ی Molecule فرمول شیمیایی یانام شیمیایی (باحروف لاتین)ترکیب موردنظرراتایپ کرده وبرروی کلمه ی submit کلیک نمایید.
1-مجموع الکترونهای لایه ظرفیت مولکول موردنظرراحساب می کنیم.
2-تعدادالکترونهای موردنیازبرای ساختارلوویس راباتوجه به قاعده هشت تایی بدست
می آوریم.
3- تعدادالکترونهای پیوندی را ازاختلاف الکترونهای لایه ظرفیت والکترونهای ساختارلوویس (مرحله1و2)تعیین می کنیم.
4-تعدادالکترونهای ناپیوندی را ازاختلاف الکترونهای لایه ظرفیت والکترونهای پیوندی (مرحله1و3)تعیین می کنیم.
5-باداشتن تعدادالکترونهای پیوندی وتعدادالکترونهای ناپیوندی ساختارلوویس مولکول موردنظررارسم می کنیم.